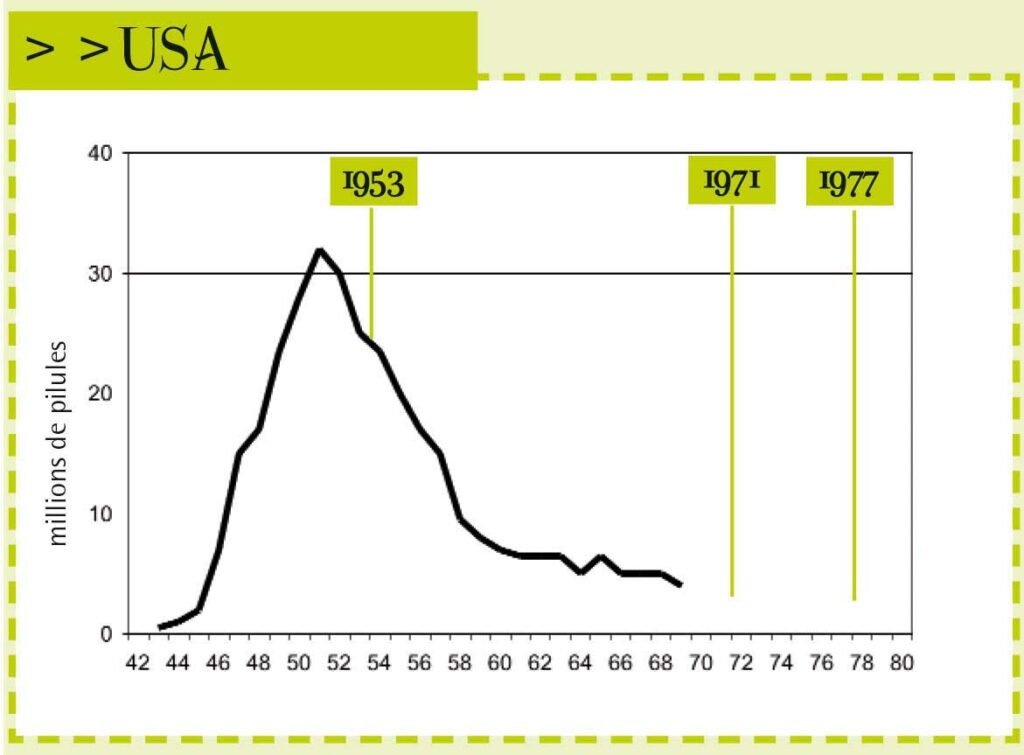
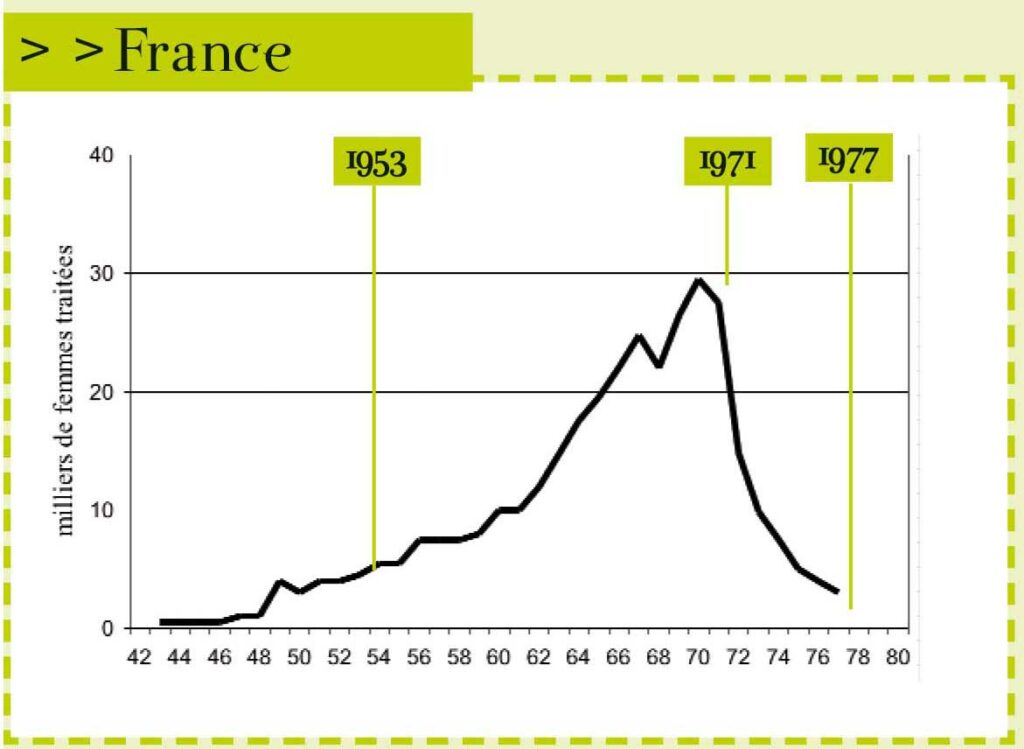
Les années 30 : découverte d’un médicament séduisant, mais à l’efficacité non prouvée, à prescrire aux femmes enceintes
Le diéthylstilboestrol (DES) est la dénomination commune internationale d’un œstrogène de synthèse découvert en 1938 par le médecin et chimiste anglais Charles Dodds. Le procédé de fabrication imaginé par Charles Dodds a le mérite d’être très peu coûteux à mettre en œuvre.
A cette époque, les biologistes montrent qu’en cas de menace de fausse couche, le taux des œstrogènes dans les urines diminue. Les médecins en déduisent que la fausse couche résulte d’un manque d’œstrogènes. Ils supposent alors qu’en donnant un supplément d’œstrogènes aux femmes enceintes, elles feront moins de fausses couches.
Il faut se souvenir qu’avant la seconde guerre mondiale, pour commercialiser un médicament, les fabricants n’avaient pas à obtenir une Autorisation de Mise sur le Marché (AMM). Il n’y avait donc pas nécessité d’effectuer d’essais cliniques rigoureux pour démontrer l’efficacité et l’innocuité d’un produit.
Le DES est alors considéré comme une « pilule miracle » permettant d’éviter les fausses couches grâce à un apport d’œstrogènes. Par extension, sa prescription est envisagée, sans preuve particulière, pour toutes sortes d’autres usages. Dans un souci philanthropique, Charles Dodds ne dépose pas de brevet et laisse ce médicament dans le domaine public (le découvreur du DES sera d’ailleurs fait Lord par la Reine Elisabeth II en 1964, en reconnaissance de son apport important à la recherche médicale).
Les années 40 : essor de la prescription dans les pays développés
A partir de 1947, suite à l’accord de la Food and Drug Administration (FDA), des centaines de firmes pharmaceutiques se mettent à commercialiser le DES, permettant la prescription du médicament à des millions de femmes enceintes dans la plupart des pays développés. En France, il a été prescrit essentiellement sous les marques suivantes :
• Distilbène® produit par le laboratoire Borne, puis à partir de 1950, par le laboratoire UCEPHA (racheté par UCB Pharma),
• Furostilboestrol® produit par le laboratoire UCEPHA (racheté par UCB Pharma),
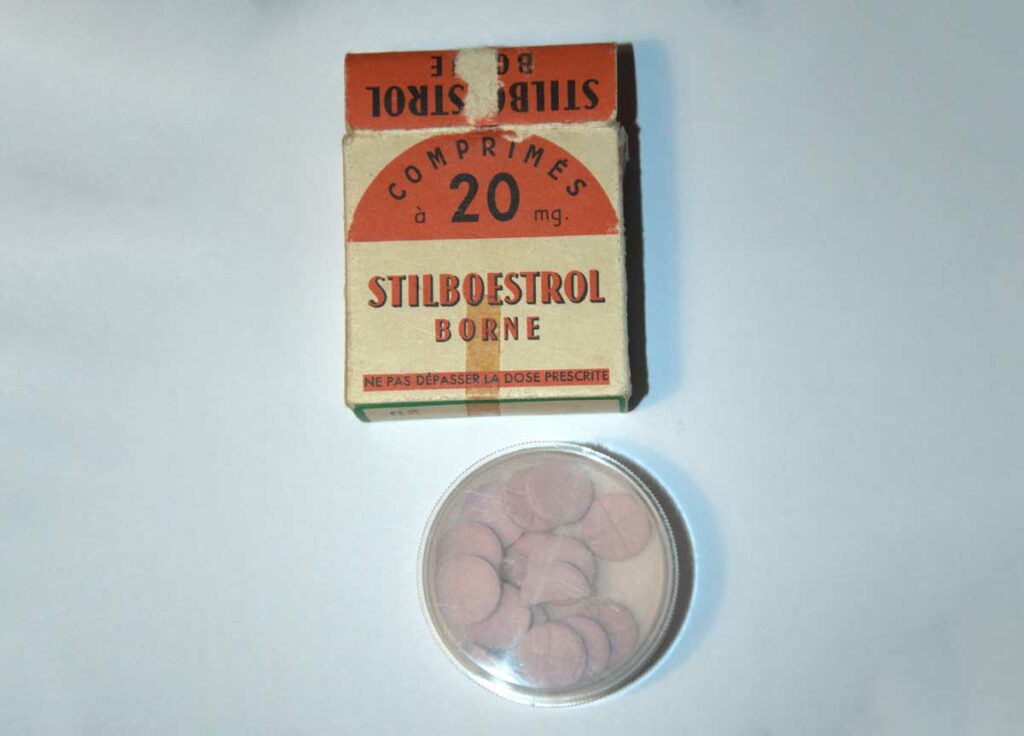
• Stilboestrol-Borne® produit par le laboratoire Borne, (aujourd’hui Novartis) jusqu’en 1974.


Les années 50 : suspicion de la dangerosité du DES aux Etats-Unis
1953 : Aux Etats-Unis, les prescriptions commencent à chuter
Le pic de prescription du DES, produit considéré jusque-là comme la prescription de référence chez les femmes enceintes, est atteint en 1952. Ensuite, le nombre des prescriptions diminue. En 1953, le Dr W. Dieckmann publie les résultats d’une étude clinique évaluant l’efficacité du DES selon un protocole d’étude particulièrement bien conçu. Il constate que le DES ne diminue pas l’incidence des accidents de grossesse et même que « les résultats semblent indiquer que le stilboestrol favorise les accouchements prématurés. Ce peut être dû à un taux hormonal excessif. ».
Il constate aussi que « bien que le taux de fausses couches soit plus élevé dans le groupe traité par stilboestrol que dans le groupe témoin, le nombre total de patientes était trop faible pour obtenir un résultat significatif». Il conclut que « le stilboestrol ne réduit pas l’incidence des fausses couches, de la prématurité ou de la postmaturité. Les bébés prématurés nés d’une mère traitée par stilboestrol ne sont ni plus ni moins matures que les bébés prématurés nés d’une mère appartenant au groupe témoin. Il ne diminue pas l’incidence de la mortalité périnatale. Il ne diminue pas la fréquence de la toxémie gravidique ». Au cours des années suivantes, d’autres œstrogènes commencent à apparaître sur le marché américain. Peu à peu, ils supplantent le DES.
Les années 60 : une progression constante des prescriptions en France
1964 – 1971 : En France, les prescriptions continuent de progresser
En France, le nombre des prescriptions de DES continue d’augmenter. Une enquête rétrospective de l’INSERM, publiée en 1983 par le Pr Spira, sur les prescriptions médicamenteuses pendant la grossesse, estimera qu’en 1964, le DES était utilisé dans 1,2% des naissances (statistiques ne tenant pas compte des prescriptions en piqures et en suppositoires).
En 1967, la notice du Distilbène® dans le dictionnaire Vidal ne comporte pas moins de cinq indications pour la femme. La même année, un embryologiste, le Pr Gabriel-Robez, signale une « action tératogène du dipropionate de diéthylstilboestrol injecté à la souris à des doses variables, du 9e au 11e jour de la gestation ». L’importance des anomalies et leur nombre sont en rapport direct avec les doses utilisées.
Au même moment, aux Etats-Unis, un médecin canadien, le Pr D.H. Carr, publie un article démontrant que les fausses couches sont liées à des problèmes génétiques. Ainsi, les chutes de taux hormonaux précédant les fausses couches spontanées ne sont pas la cause mais la conséquence de l’arrêt de ces grossesses, invalidant du même coup les hypothèses qui, vingt ans plus tôt, avaient servi d’argument pour la prescription du DES chez les femmes enceintes.
Les années 70 : Lente prise de conscience de la nécessité d’arrêter les prescriptions pour les femmes enceintes
1971 : Aux Etats-Unis, contre-indication aux femmes enceintes
En 1971, l’apparition alarmante de cas de cancers (Adeno-Carcinome à Cellules Claires ou ACC) du vagin ou du col utérin chez de jeunes femmes âgées de 14 à 22 ans, mettent la communauté médicale en alerte. Ce cancer très rare n’a jamais été observé chez des femmes aussi jeunes. Le journal médical américain New England Journal of Medecine fait mention d’un lien possible entre le DES et le cancer à cellules claires chez des jeunes femmes exposées in utero au DES prescrit à leur mère (Herbst A et col.).
Le Ministre de la santé des Etats-Unis met en garde contre l’utilisation du DES pendant la grossesse. Le Dr Arthur Herbst établit un registre international des cas de cancers à cellules claires. Sept mois plus tard, la FDA recommande aux médecins de cesser de prescrire du DES aux femmes enceintes. Le Canada fait de même peu après.
1977 – Un médicament contre-indiqué en France chez les femmes enceintes
En Europe, l’Angleterre interdit le DES en 1973, la Belgique et les Pays-Bas en 1975, l’Irlande en 1976. Les informations alarmantes se multiplient.
En 1974, J. Henry-Suchet fait la première communication sur des cas d’adénose vaginale.
En 1975, l’équipe du Pr J. Barrat publie un des premiers cas français d’adénocarcinome du vagin. La publication est accompagnée d’une mise en garde préventive. En France, l’indication du Distilbène pour traiter les avortements spontanés et à répétition est supprimée en 1976.
En 1977, le dictionnaire Vidal, révisé par la « Commission Alexandre » est devenu la référence française officielle en matière d’information sur les médicaments. Il mentionne que le DES est contre-indiqué chez la femme enceinte. Malgré ces interdictions, le DES continue d’être prescrit dans certains pays jusqu’au milieu des années 80. En France, le Distilbène a été prescrit sporadiquement au-delà de 1977.
Article “actualité” à mettre en lien avec la Commission Alexandre.
Les années 80 : Les associations de victimes apparaissent et travaillent depuis, à faire reconnaître et diffuser l’information
1980 – Le DES n’est plus prescrit chez les femmes enceintes
A partir de 1980, le DES restera utilisé dans le monde dans certaines indications : traitement substitutif de la ménopause, blocage de la lactation, cancer de la prostate, pilule du lendemain, traitements de l’acné et des problèmes gynécologiques, préparation des transsexuels au changement de sexe, ralentissement ou accélération de la croissance des jeunes filles et garçons, et comme stimulateur de croissance du bétail.
En France, le diéthylstilboestrol est resté commercialisé jusqu’en 2018 sous le nom de Distilbène, uniquement dans l’indication de certaines pathologies prostatiques.
Depuis 1980 – Information et prise en charge des patientes exposées
L’administration à grande échelle de DES aux femmes enceintes jusqu’en 1980 a, maintenant encore, des conséquences sur les générations suivantes, notamment sur les « filles DES » qui ont souhaité des enfants, de nombreuses années après leur exposition au DES pendant la grossesse… de leur maman.
Il faut prendre en charge ces personnes et être à l’affût de conséquences médicales ignorées.
Peu à peu, partout dans le monde, des groupes de patients sont créés par des personnes directement concernées estimant que l’information sur les conséquences du DES est insuffisante, réductrice et souvent erronée, voire même inexistante. Parfois, il faut lutter contre le déni. Ainsi, en Australie, où l’usage du DES a été très largement répandu, lorsqu’à la demande du « groupe DES Action » le Ministère de la Santé a ouvert une « clinique DES » à Victoria, beaucoup de gynécologues australiens ont prétendu que la prescription du DES ne concernait que la ville de Victoria. On pourrait très facilement décrire les mêmes sortes de dénégations dans tous les pays développés, notamment en France.
Années 90 : le DES, modèle reconnu de perturbateur endocrinien
Le concept de perturbateur endocrinien est né de découvertes qui se sont à un moment cristallisées lors d’une conférence réunissant 21 chercheurs, en 1991, à Wingspread, dans le Wisconsin. A l’issue de cette conférence, les participants ont publié une déclaration qui est à la source des nombreux développements d’aujourd’hui sur les perturbateurs endocriniens. L’exposition in utero au DES figure dans ce texte.
EXTRAITS DE LA DECLARATION DE WINGSPREAD
Altérations du développement sexuel induites par les produits chimiques : le sort commun des animaux et des hommes
« (…) Un grand nombre de produits chimiques de synthèse libérés dans la nature, ainsi que quelques composés naturels, sont capables de dérégler le système endocrinien des animaux, y compris l’homme. Il s’agit notamment des composés organochlorés, qui, du fait de leur persistance, s’accumulent dans les chaînes alimentaires. Ceux-ci comprennent certains pesticides (fongicides, herbicides et insecticides) et produits chimiques, ainsi que d’autres produits synthétiques et certains métaux (…).
De nombreuses populations d’animaux sauvages sont d’ores et déjà affectées par ces composés.
(…) Les humains sont également affectés par ces composés. Le distilbène, un médicament de synthèse, et beaucoup de composés cités en note ont des effets oestrogéniques. Les femmes dont les mères ont ingéré du distilbène sont particulièrement touchées par le cancer du vagin, par diverses malformations de l’appareil reproducteur, par des grossesses anormales et des modifications de la réponse immunitaire. Les hommes et les femmes exposés pendant leur vie prénatale présentent des anomalies congénitales de l’appareil reproducteur et une baisse de fertilité. Les effets observés chez les victimes du distilbène sont semblables à ce que l’on observe chez les animaux contaminés, dans la nature et en laboratoire. Cela suggère que les humains partagent les mêmes risques. (…)»
« (…) Pour de nombreuses raisons, il faudrait réétudier les victimes du distilbène. (…) Le distilbène pourrait fournir le modèle le plus extrême pour rechercher les effets de substances oestrogéniques moins puissantes. Ainsi, les marqueurs biologiques déterminés chez les victimes de cet oestrogène synthétique permettront d’étudier les effets résultant de la contamination ambiante. »
(Rédigé à partir du rapport sénatorial « Perturbateurs endocriniens, le temps de la précaution ». Rapport n° 765 (2010-2011) de M. Gilbert BARBIER, fait au nom de l’Office parlementaire d’évaluation des choix scientifiques et technologiques, déposé le 12 juillet 2011. L’intégralité de la Déclaration de Wingspread est consultable ici ; tandis que ce lien-ci vous renverra au sommaire du rapport.)
Les années 2000 : Le DES reconnu comme étant un problème de santé publique
En 2005, Réseau D.E.S. France a obtenu du Ministère de la Santé la création, pendant un an, d’un groupe de travail officiel, chargé de faire des propositions pour l’amélioration de la prise en charge des victimes du DES (arrêté paru au Journal Officiel du 19 juillet 2005).
Depuis 2010 : Le DES devient sujet d’étude – la pharmacovigilance, sujet de société
L’histoire du DES montre que les effets indésirables des médicaments peuvent s’inscrire dans la durée, sur plusieurs générations. D’où l’importance d’études de pharmacovigilance sur le long terme, menées par des équipes indépendantes.
Depuis plusieurs années, le DES intéresse aussi les sciences sociales. Citons en particulier les travaux réalisés par :
- les sociologues Emmanuelle Fillion et Didier Torny,
- ainsi que par Coline Salaris, Docteure en sciences politiques.
- et Giulia Colavolpe Severi, auteure de l’article
L'épée de Damoclès(https://journals.openedition.org/ateliers/11135)
Années 2020 : utilisation du DES dans l’élevage dans différents pays
L’utilisation des oestrogènes dans l’élevage a été interdite en France en 1959 (Décret n°59-450 du 20 mars 1959).
Chine
Depuis quelques années, nous constatons la publication régulière d’études scientifiques portant sur la mise au point de techniques fiables, peu onéreuses et faciles à mettre en oeuvre, pour détecter de traces de DES dans l’eau des rivières, la chair des poissons, le lait de vache, la viande… (exemples : Chen 2011, Yang 2020).
Il est à noter que le DES n’est que depuis peu de temps interdit en Chine comme “complément alimentaire” dans l’élevage et l’aquaculture.
Une observation appelle un commentaire sur d’autres publications récentes :
- Les unes rapportent des séries de cancers ACC sans prescription de DES prénatale (Jiang 2014).
- D’autres démontrent la présence de perturbateurs endocriniens, dont le DES, à des niveaux significatifs dans les urines humaines (Zhang 2017). Ainsi, les femmes qui n’ont pas été exposées par une prescription de DES en cours de la grossesse de leur mère, sont peut-être exposées de nos jours par la nourriture consommée par les femmes enceintes.
Iran, Turquie
Des équipes de ces pays ont publié des études portant sur des méthodes de détection de DES dans l’eau des rivières (Ghasemi 2017), ou la présence de DES dans la viande (Sever 2012).
Références
Chen XB, Wu YL, Yang T. Simultaneous determination of clenbuterol, chloramphenicol and diethylstilbestrol in bovine milk by isotope dilution ultraperformance liquid chromatography-tandem mass spectrometry. J Chromatogr B Analyt Technol Biomed Life Sci. 2011 Apr 1;879(11-12):799-803. doi: 10.1016/j.jchromb.2011.02.030. Epub 2011 Feb 25. PMID: 21397571.
Yang X, Wang Y, Song C, Hu X, Wang F, Zeng X. Hapten Synthesis and the Development of an Ultrasensitive Indirect Competitive ELISA for the Determination of Diethylstilbestrol in Food Samples. Sci Rep. 2020 Feb 24;10(1):3270. doi: 10.1038/s41598-020-59112-1. PMID: 32094434; PMCID: PMC7039971.
Jiang X, Jin Y, Li Y, Huang HF, Wu M, Shen K, Pan LY. Clear cell carcinoma of the uterine cervix: clinical characteristics and feasibility of fertility-preserving treatment. Onco Targets Ther. 2014 Jan 9;7:111-6. doi: 10.2147/OTT.S53204. PMID: 24470762; PMCID: PMC3891640.
Zhang D, Zhou L, Lei Y, Zhou Z, Zhou J, Chen S. Investigation of diethylstilbestrol residue level in human urine samples by a specific monoclonal antibody. Environ Sci Pollut Res Int. 2017 Mar;24(8):7042-7050. doi: 10.1007/s11356-017-8405-y. Epub 2017 Jan 14. PMID: 28092005.
Ghasemi A, Asgarpour Khansary M, Marjani A, Shirazian S. Using quantum chemical modeling and calculations for evaluation of cellulose potential for estrogen micropollutants removal from water effluents. Chemosphere. 2017 Jul;178:411-423. doi: 10.1016/j.chemosphere.2017.02.152. Epub 2017 Mar 3. PMID: 28342373.
Sever E, Okumus B, İnce S. Erzurum Yöresinde Satışa Sunulan Kırmızı Etlerde 17 β-östradiol, Dietilstilbestrol ve Zeranol Kalıntılarının Araştırılması. Kafkas Univ Vet Fak Derg. 18 (2): 267-272, 2012 DOI:10.9775/kvfd.2011.5404
Zamora-León P. Are the Effects of DES Over? A Tragic Lesson from the Past. Int J Environ Res Public Health. 2021 Sep 30;18(19):10309. doi: 10.3390/ijerph181910309. PMID: 34639609; PMCID: PMC8507770.